Certificado de Liberación de Lotes
La liberación de lote de productos biológicos: vacunas o derivados de plasma humano es un proceso de carácter obligatorio antes de su distribución o comercialización o uso en el mercado peruano, la cual es aprobada mediante la expedición del certificado de liberación de lote por la ANM.
Registro Sanitario
La solicitud de expedición del certificado de liberación de lote se presenta por cada lote y por cada ingreso al país de un mismo lote.
El artículo 4 del Decreto Supremo N° 016-2018-SA, Reglamento que regula la expedición del Certificado de Liberación de lote de productos biológicos: Vacunas o Derivados del Plasma Humano, establece que la Liberación de Lotes de los productos biológicos mencionados es un proceso de carácter obligatorio antes de su distribución o comercialización o uso en el mercado peruano, la cual es aprobada mediante la expedición del Certificado de Liberación de Lote otorgado por la Autoridad Nacional de Productos Farmacéuticos, Dispositivos Médicos y Productos Sanitarios. En tal sentido, a efectos de solicitar el certificado de Liberación de Lote, considerar lo estipulado en los artículos 10 y 11 del Decreto Supremo N° 016-2018-SA, el que será tramitado a través de Mesa de partes Virtual.
Para acceder al formato de solicitud de autorización de lote:
- Autorización excepcional para la liberación de lote:
La ANM autoriza la distribución o uso o comercialización sin expedición del certificado de liberación de lote en:
-
- Situaciones de urgencia o emergencia declarada en el país.
- Situaciones de Salud pública
Para acceder al formato de solicitud de autorización excepcional:
- Vacunas y Derivados del Plasma Humano de fabricación Nacional
En aquellos casos que se solicite la liberación de lote de una vacuna o derivado de plasma humano de fabricación nacional, deberá cumplir con la realización de los controles de calidad respectivos por el Centro Nacional de Control de calidad del Instituto Nacional de Salud, según la normativa vigente.
-
- Información sobre el proceso de control de calidad:
- Red Nacional de Laboratorios oficiales de Control de Calidad – INS
Se tiene disponible para la orientación al usuario para los procesos de liberación de lote la Guía de apoyo al usuario a través de:
Registro Sanitario condicional
En el caso de vacunas y derivados de plasma humano autorizados para la prevención y tratamiento de enfermedades gravemente debilitantes o potencialmente mortales que den lugar a una emergencia declarada, para la aplicación de liberación de lote se considera lo estipulado en el art 37 y art 38 del Decreto Supremo N° 020-2023 -SA Reglamento para el Registro Sanitario Condicional de Medicamentos y productos Biológicos (entra en vigencia desde el 19/01/2024), Decreto Supremo N° 002-2021-SA Decreto Supremo que aprueba el Reglamento para el Registro Sanitario Condicional de Medicamentos y Productos Biológicos y modificatoria, (vigente hasta el 18/01/2024).
- Autorización excepcional para la liberación de lote:
La ANM autoriza la distribución o uso o comercialización sin expedición del certificado de liberación de lote en:
-
- Los casos en que el formato de protocolo resumido de producción y control del producto se haya incluido como obligación específica
Para acceder al formato de solicitud:
-
- Certificado de liberación de lote de Vacuna o derivado de plasma humano con registro sanitario CONDICIONAL o autorización excepcional:
- Informe Anual de producto Biológico
La normativa del Registro Sanitario condicional en su art. 39 establece que el titular del Registro Sanitario condicional a partir de otorgado el referido registro presenta cada año a la ANM el informe anual de productos biológicos, esto a fin de verificar la consistencia de todos los lotes fabricados.
- Procedimientos TUPA:
- Procedimiento PA99000983: Autorización excepcional para la liberación de lote de productos biológicos: vacunas o derivados de plasma humano con registro sanitario condicional.
- Procedimiento PA99005A22: Certificado de Liberación de Lote de productos biológicos: vacunas o derivados de plasma humano con registro sanitario condicional
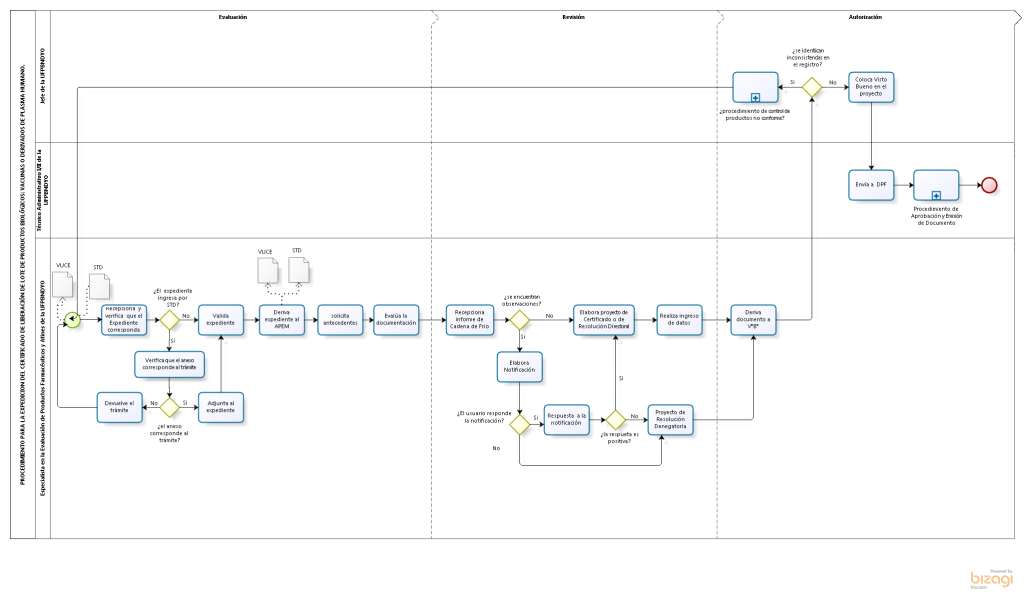
Las Solicitudes de Certificado de Liberación de Lote son evaluadas por el Equipo de Productos Biológicos /Área de Liberación de lote de vacunas y derivados de plasma humano, asimismo interviene en el proceso el Equipo de Control y Vigilancia de Productos / Área de Pesquisa y envío de muestra, en cumplimiento de la normatividad vigente que es de aplicación obligatoria para la obtención del certificado o autorización excepcional de liberación de lote.
Normatividad
- Decreto Supremo N° 016-2018/SA Aprueba Reglamento que regula la expedición del certificado de liberación de lote de productos biológicos: vacunas o derivados de plasma humano.
- D.S. 016-2011 –SA Reglamento para el registro, control y vigilancia sanitaria de productos farmacéuticos, dispositivos médicos y productos sanitarios
- Resolución Directoral N° 005-2019-DIGEMID-DG-MINSA Aprueban Formato “Certificado de Liberación de Lote de Producto Biológico
- Decreto Supremo N° 020-2023-SA Reglamento para el Registro Sanitario Condicional de Medicamentos y productos Biológicos
- Decreto Supremo N° 002-2021-SA Decreto Supremo que aprueba el Reglamento para el Registro Sanitario Condicional de Medicamentos y Productos Biológicos y modificatoria.
Actualizado el 05/06/2025
- Vacunas
- Año 2025
- Año 2024
- Año 2023
- Año 2022
- Año 2021
- Año 2020
- Año 2019
- Derivados del plasma humano
- Año 2025
- Año 2024
- Año 2023
- Año 2022
- Año 2021
- Manual de entrenamiento : concesión de licencias, liberación de lotes y disponibilidad de laboratorios/WHO/V&B/01.16 (OMS)
- Guía para Liberación de Lote independiente de vacunas por Autoridades reguladoras (OMS)
- Anexo 2 Guía para Liberación de Lote independiente de vacunas por Autoridades reguladoras (OMS)
